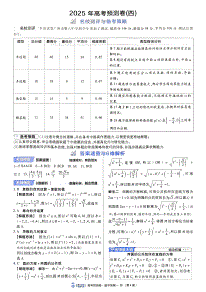
#(##学年第一学期浙江强基联盟!高三年级化学试题参考答案!+选*#+选,-+稀释浓硫酸时!要把浓硫酸缓缓地沿器壁注入水中!同时用玻璃棒不断搅拌!以使热量及时地扩散一定不能把水注入浓硫酸中图中所示操作错误#.+标签应在上!在下有可能被残留液腐蚀#*+闻气体或液体的气味时!都应用手在瓶口轻轻地扇动!使极少量的气体飘进鼻子中!为防止中毒!不能将鼻子凑到集气瓶口去闻太多气体的气味!图中所示操作不正确#,+用坩埚钳夹取灼热的坩埚时!必须将钳尖先预热!以免坩埚因局部冷却而破裂!且钳尖朝上!利用中间的圆形部位托住坩埚#$+选*-+锌为$(号元素!-错误#.+图示为乙烯的结构简式#*+铁原子$/0)1#!铁离子$1#$20$/3!故铁离子的最外层电子轨道表示式正确#$$$$$$$,+次氯酸电子式为4$5$*6$!,错误#$$$$)+选--+结构相似%组成上相差若干的有机化合物为同系物!乙二醇&45*4#*4#54'是饱和二元醇!甲醇是饱和一元醇!两者虽均含(54!但所含官能团&(54'数目不同!不互为同系物!-错误.+质子数相同%中子数不同的核素互为同位素!!)7的质子数为!中子数为!!37的质子数为!中子数为8!两者质子数相同%中子数不同!互为同位素!.正确*+由同种元素组成的不同的单质互为同素异形体!90和98是由硫元素组成的不同的单质!两者互为同素异形体!*正确分子式相同%结构不同的化合物互为同分异构体!$#3和5&!二氧六环'的分子式,+*4*55*45!)%&*)485#'相同!但结构不同!两者互为同分异构体!,正确#3+选*-+石油不仅有液态烃!还有少量气态烃%固态烃-错误.+在自然界中!*5#的吸收转换不只有光合作用!还有别的形式!如*:*5$;4#5;*5####*:&4*5$'#等!.错误*+将橡胶和高吸水性树脂转变为网状结构的主要目的是不同的!前者主要是为了增大强度!后者主要是既吸水又不溶于水!*正确,+葡萄糖的氧化%酸碱中和是放热反应!大豆的综合利用的途径往往包括蛋白质与油脂等方面!是正确的!但碳酸钙的分解是吸热反应!,不正确#0+选,;%$-+74);75####7#%;#4#5$.+07:;#7:75####7#%;)7:#5*+)74$;$5#####7#;04#5,+*5&74#'#;#7:54####74$%;7:#*5$所以选,#+选*!高三化学参考答案!第!!页#共页$%#$%&'()*书-+在$.<&$;34#5###.<#;4.<5$;5#%;=4&的反应中!发生化合价变化的元素有.<%5二种元素!而&%4元素的化合价没有发生变化!故在该反应中!只有两种元素化合价发生改变!错误.+在该反应中!.<元素的化合价由反应前.<&$中的;$价变为反应后.<#中的(价!化合价降低!获得电子!所以该反应的氧化剂为.<&$!而.<#是还原产物.<元素的化合价由反应前.<&$中的;$价变为反应后4.<5$中的;3价!化合价升高!失去电子!被氧化!.<&$是还原剂!4.<5$是氧化产物5元素的化合价由反应前4#5中的%#价变为反应后5#中的(价!化合价升高!失去电子!所以4#5是还原剂!5#是氧化产物!即该反应的氧化产物有4.<5$和5#!错误*+3>?64#5参加反应只有#>?64#5作还原剂!#>?64#5只还原了#)$>?6.<&$!所以!@3>?64#5参加反应!(@0>?64#5作还原剂只还原(@)>?6.<&$!*正确,+根据方程式可知*每有$>?6.<&$发生反应!有0>?6电子转移!则若有!@3>?6.<&$参加反应!有$>?6A%转移!错误#8+选*-+重结晶法提纯苯甲酸的前三步是!加热溶解!趁热过滤!#冷却结晶!再过滤%洗涤%干燥%称重!-错误.+碱性条件下只会看到红褐色沉淀!.错误*+受强酸或强碱腐蚀致伤时!应先用大量水冲洗!降低浓度!然后相应地用弱碱性物质&碳酸氢钠溶液'或弱酸性物质&饱和硼酸溶液'清洗!最后用水冲洗!并视情况做进一步处理!*正确,+亚铁离子加热过程中易被氧化!该盐结晶水也会失去!所以在小火加热!蒸发浓缩至溶液表面出现晶膜时!将其静置!自然冷却!,错误#=+选.-+没指出+标准状况,*+乙烯和环丙烷的摩尔质量不同!故分子总数无法确定,+标准状况下!*9#是液体上述-%*%,均错误;.+7:与4*6反应!再与4#5反应!即)@0B7:完全反应!相当于(@#>?67:变成7:!即转移(@#!-电子!.正确#!(+选,-+放电时为原电池!质子向正极移动!电极:为负极!则该电池放电时质子从电极:移向电极C!-错误%;.+酸性条件下!氧气得电子与氢离子反应生成水!电极C附近发生的电极反应为5#;)A;)4####4#5!.错误%#%;*电极:为负极!发生氧化反应!电极反应为95#;#4#5%#A###95);)4!硫酸应当拆为离子形式!*错误#%;,+由总反应式#95#;5#;#4#5####95);)4可知!放电过程中消耗的95#和5#的体积比为#D!!,正确#!!+选,-+它的单体是*&*4#54')和*&*554').+醇酸脱水缩合形成酯类高分子化合物*+它含有八元环结构上述-%.%*错误#它的单体!先由$>?6甲醛与!>?6乙醛在碱性条件下羟醛缩合生成&*4#54'$*45!再与氢气加成生成季戊四醇-*&*4#54').!&*4#54'$*45氧化生成*&*554')!所以,正确#!#+选,;;&!'由于7:的离子半径大于EF的离子半径!7:#5的离子键强度弱于EF#5&#'一般金属失电子生成金属阳离子是吸热的&需消耗能量'!$3&(!而非金属得电子生成阴离子&更加稳定'是放热的!$)'(&$'$$&(&晶体吸热变气体'%$#&(&断键吸热'&)'根据盖斯定律!$!G$#;$$;$);$3;$0#所以!$#&(!$)'(!-错误7:易失电子!吸收热量少!$3&7:#5''$3&EF#5'!.错误$0'(!生成EF#5放出热量多!$0&7:#5'&$0&EF#5'!*错误$!&$);$3;$0!,正确#!高三化学参考答案!第!#页#共页$%#$%&'()*!$+选.%%;%.发生的并非双水解反应!而是4*5$的酸性强于-6&54'$!4*5$提供4!使-65#转变成白色沉淀*%%#%-65#;4#5;4*5$###-6&54'$(;*5$#!)+选*-+化学平衡是动态平衡!不可能为(!-不正确.+升高温度可以增大反应速率!.不正确*+增大压强可以提高反应速率!*正确,+可逆反应有一定的限度!转化率不能达到!((H!,不正确#!3+选.*的浓度变化为(@0>?6$E%!!则*的速率为(@$>?6$E%!$1I!!-的速率也是(@$>?6$E%!$1%!!.的速率是(@!3>?6$E%!$1I!!根据计算-的转化率为$(H!#1时物质.的浓度为(@>?6$E%!即!%正确#!0+选.根据已知!五种元素是同周期主族元素!又'的最外层电子数是J次外层电子数的$倍!J有二个电子层!次外层为#个电子!'为氧元素又据盐的结构图示可知!K形成四个共价键!且与氧&''形成双键!K原子的最外层电子数为)!K为碳元素L形成一个共价键!L为氟元素盐中含有草酸根结构且与J相连%J还与二个&相连!J为硼元素电池材料中M;为非8电子稳定结构!M为锂元素#据此!原子半径*&'5'*!正确简单气态氢化物!沸点4&'4#5&均存在氢键!而每个水分子平均有二个氢键'!但热稳定性*4#5'4&&原子半径&小!4(&键牢固'!-错误同周期元素原子半径随原子序数增加而增大!简单阴离子半径亦然!.正确锂的密度比煤油小!它不可以保存于煤油中!硼化氢通常表示为.#40!*错误J的最高价氧化物对应的水化物是4$.5$!是一元弱酸!,错误#!+选,-+由图可知!有!个N结合$个9为;$价!其他$个N结合!个9都是;!价!正价总数为;0!而9为%#价!故-错误.+该分子中全部为单键!含有N(N非极性键!故.错误*+三硫化四磷属于分子晶体!相对分子质量大于N)!则三硫化四磷的熔点较高!所以该物质的熔%沸点比N)高!故*错误,+)N4$;$95####N)9$;04#5!故,正确#!8+选,-+由于4*7酸性弱!7:*7溶液的碱性较强!24大于!!所标曲线为7:54滴定4*7!由于甲基橙的变色范围是24在$@!到)@)之间!因此滴定4*7时!不宜选用甲基橙作为指示剂!-错误.+处溶液24'!溶液呈酸性!醋酸电离为主!抑制水的电离!#处溶液24G!此时存在*4$*557:和少量的*4$*554!%处为滴定终点!溶液中恰好生成*4$*557:!*4$*557:水解促进水的电离!因此溶液中水的电离程度*'#'%!.错误*+#处溶液的24G!溶液呈中性!溶液中#&4;'G#&54%'!对于所滴定的醋酸溶液!根据电荷守恒!;;%%;%;%#&7:';#&4'G#&54';#&*4$*55'!由于#&4'G#&54'!则#&7:'G#&*4$*55'!此时滴;加7:54的体积不到#(>E!因此溶液中还存在极少量的*4$*554!则浓度关系应为#&7:'G%#&*4$*55'&#&*4$*554'!*错误%,+点!的溶液中存在*4$*557:和*4$*554!根据物料守恒!#&*4$*55';#&*4$*554'G(@(3>?6$E%!!点溶液中存在7:*7和4*7!根据物料守恒!#&4*7';#&*7%'G(@(3>?6$E%!!两溶%%%%液混合!则有#&*4$*55';#&*4$*554'G#&4*7';#&*7'!即#&*4$*55'%#&*7'G#&4*7'%#&*4$*554'!故,正确#!=+选*-+采用KO.<#)9F5#为催化剂!通过氧溴化可将甲烷转化为一溴甲烷!反应过程中有甲烷和溴的反应!只要在光照条件下!就会发生连续取代!产物中可能混有*4#.<#等!-正确.+若用&A.<#替换KO.<#!&A.<#中铁元素显;#价!能与氧气等反应生成&A5!&A5的活泼性比KO5差&甚!高三化学参考答案!第!$页#共页$%#$%&'()*至生成&A#5$等'!因此可能一溴甲烷的产率将降低!.正确*+过程&中反应方程式为#4.<;5#;KO.<####4#5;#.<#;KO5!氧化剂为5#!还原剂为4.<%KO.<#!氧化剂与还原剂的物质的量之比为!D$!*错误!选*,+由反应机理图可知!反应过程中加入的有4.<%5#%*4)!生成的有*4$.<%4#5!KO.<#%KO5%.<#在参与催化剂循环!故总反应为#*4);#4.<;5#***)#*4$.<;#4#5!,正确#$#(+选,-+&A$;不能与加入的硫酸发生氧化还原反应!-错误&注*褪色是另外有原因'.+碳酸钠溶液中加入稀盐酸生成的二氧化碳气体中可能混有4*6!4*6与硅酸钠反应生成硅酸!不能证明*%9F非金属性强弱!又非金属性氯&碳的验证!要用4*65)!.错误*+浓硫酸加入浓硝酸中放热!导致硝酸受热分解生成75#气体!不能比较氧化性!*错误,+甲苯使酸性高锰酸钾溶液褪色!甲烷不能!则说明苯环对甲基产生影响!,正确##!+&!'$/!()1!&!分'*P'*'7'&&!分'$&#'*4$74#&!分'12&!分'&$'*Q&#分!选对一个给!分!一旦有错不给分'&)'8&!分'*P$7&!分'&小球为7!大球为*P'&#分'!精准解析与关键突破&!'*P为#=号元素!基态*P原子的核外电子排布式为!1##1##20$1#$20$/!()1!!基态铜原子价层电子排布式为$/!()1!*P为金属元素!第一电离能最小!同周期自左至右第一电离能呈增大的趋势!所以四种元素第一电离能从小到大为*P'*'7'&&#'*4$74#分子中存在7(4键!所以分子间存在氢键!沸点较高*4$74#分子中7原子与*原子形成一个'键!与两个4原子分别形成一个'键!还有一对孤电子对!所以价层电子对数为)!为12$杂化#;&$'*P提供空轨道!74$分子提供孤电子对形成配位键!74$分子内部都存在共价键!
化学FX04C答案
你可能还喜欢
购买VIP会员享超值特权
VIP专享免费下载,付费文档最高省50%
免费下载
付费折扣
身份标识
文档工具
限时7.4元/月购买VIP