【化学答案及解析】1.【答案】C【解析】A.已知合金的硬度大于成分金属,即铝合金硬度大于铝单质;B.“素纱禅衣”主要成分是蚕丝,蚕丝的组成为蛋白质,蛋白质是混合物既不是电解质也不是非电解质;C.陶瓷是人类应用最早的硅酸盐材料,且陶瓷具有不导电的特性,现代生活中可采用陶瓷做高压输电线路的绝缘材料;D.燃煤中添加生石灰可减少SO2的排放,但不能减少二氧化碳的排放,对“碳中和”目标的实现无影响;故答案为:C。2.【答案】D【解析】A.SnCl2中Sn有一对孤对电子,价层电子对数为3,故其VSEPR模型为:;B.甲醛中存在C=O,其中一个π键一个σ键,π键的电子云轮廓图:;C.碳化钙是离子化合物,碳化钙和水反应生成乙炔和氢氧化钙,根据乙炔的结构可知,碳化钙中存在碳碳三键,电子式为:;D.邻羟基苯甲醛,羟基氢与醛基上的氧原子形成分子内氢键:,这样的分子内氢键形成六元环,D错误;故选D。3.【答案】A【解析】A.通过凝固法制备硫晶体在蒸发皿中进行,故选:,A正确;B.碳化钙为粉末状,不能用启普发生器制乙炔,B错误;①C.测定中和反应热需要烧杯、温度计、滴定管,不需要锥形瓶,C错误;D.重结晶法提纯苯甲酸,需要蒸发皿和漏斗,不需要温度计,D错误;故选A。4.【答案】D【解析】A.对比邻氨甲酰苯甲酸和邻苯二甲酰亚胺结构可知反应是取代反应,A错误;B.邻氨甲酰苯甲酸分子含酰胺基(-CONH2)和羧基(-COOH)这两②种官能团,B错误;C.邻苯二甲酰亚胺分子式为C8H5O2N,C错误;D.邻苯二甲酰亚胺水解生成邻苯二甲酸,1mol邻苯二甲酰亚胺与足量NaOH溶液反应最多可消耗2molNaOH,{#{QQABAYIEggioAAIAAAgCUQUQCgCQkhGCASgOQAAAoAAACQFABCA=}#}D正确。5.【答案】C【解析】A.C16S8是分子晶体,熔点由范德华力大小决定,故A错误;B.C16S8完全燃烧的产物分别为CO2和SO2,CO2为非极性分子,SO2为极性分子,故B错误;C.由分子结构可知,一个分子中σ键的数目为32,π键的数目为8,故分子中的σ键和π键的数目比为4:1,故C正确;D.C16S8分子中没有能形成氢键的原子,H2为分子晶体,故二者之间的作用是范德华力,故D错误;6.【答案】C【解析】【详解】A.醛基和碳碳双键都会和溴单质反应,故溴水褪色不能说明丙烯醛中含碳碳双键,A错误;B.挥发的盐酸也会和硅酸钠生成硅酸沉淀,产生白色沉淀不能说明碳的非金属性比硅强,B错误;C.溶液变为紫红色,说明二价锰被PbO2氧化为高锰酸根离子,体现PbO2的氧化性,C正确;D.烧杯壁变凉说明Ba(OH)28H2O与NH4Cl晶体反应为吸热反应,则正反应活化能比逆反应的大,D错误;7.【答案】C【解析】【详解】A.氯酸钾与浓盐酸制氯气时,氯酸钾为氧化剂,6份HCl中有5份作还原剂,另外一份起到酸性的作用,即氯气分子中既含有37Cl,又含有35Cl,而生成物KCl中只含35Cl,A项错误;.溶液与溶液等体积混合,C0.01mol/LNH4AlSO420.02mol/LBaOH23+22+nNH4:nAl:nSO4:nBa:nOH1:1:2:2:4,恰好完全反应生成、、,方程式BaSO4AlOH3NH3H2O为3+22+,项正确;NH4+Al+2SO4+2Ba+4OH=2BaSO4+AlOH3+NH3H2OC8.【答案】A【解析】【分析】根据图示可知W形成1个共价键,又是四种元素中原子序数最小的元素,X形成4个共价键且W、X、Z分别位于不同周期,且Z的原子半径在同周期元素中最大,则W是H元素,X是C元素,Z是Na元素,Y形成2个共价键,原子序数比C大,比Na小,则Y是O元素。【详解】A.H和C形成的化合物常温可能为气态、液态或固态,不一定比H和O形成的化合物的沸点低,A项错误;B.O2、Na的核外电子排布相同,核电荷数越大,离子半径越小,所以简单离子半径:Z
广西南宁市第二中学2024-2025学年高三上学期11月月考化学答案
你可能还喜欢
购买VIP会员享超值特权
VIP专享免费下载,付费文档最高省50%
免费下载
付费折扣
身份标识
文档工具
限时7.4元/月购买VIP
相关推荐
-
广西南宁市第二中学2024-2025学年高三上学期11月月考生物答案
2024-12-12 21:48
 4页
4页 -
广西南宁市第二中学2024-2025学年高三上学期11月月考生物
2024-12-12 21:48
 6页
6页 -
广西南宁市第二中学2024-2025学年高三上学期11月月考数学
2024-12-12 21:48
 5页
5页 -
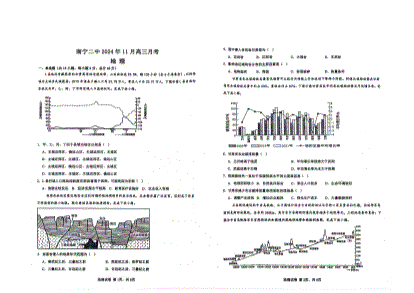
广西南宁市第二中学2024-2025学年高三上学期11月月考地理
2024-12-12 21:48
 3页
3页 -
广西南宁市第二中学2024-2025学年高三上学期11月月考化学
2024-12-12 21:48
 9页
9页 -
广西南宁市第二中学2024-2025学年高三上学期11月月考数学答案
2024-12-12 21:48
 20页
20页 -
广西南宁市第二中学2024-2025学年高三上学期11月月考英语答案
2024-12-12 21:48
 1页
1页 -
广西南宁市第二中学2024-2025学年高三上学期11月月考语文
2024-12-12 21:48
 10页
10页













